 400-780-8018
400-780-8018咪唑并吡啶类(Imidazopyridine Derivatives)是一类重要的含氮稠合杂环化合物,因其优异的结构稳定性和多样化的取代方式,在医药、农药及染料等行业中具有广泛应用。由于其与吲哚、氮杂吲哚等骨架具有一定的结构相似性,该类化合物在药物化学领域长期受到关注。
常见的咪唑并吡啶结构类型包括:咪唑并[1,2-a]吡啶、咪唑并[4,5-b]吡啶、咪唑并[4,5-c]吡啶及咪唑并[1,5-a]吡啶等。不同的稠合方式赋予化合物不同的电子特性和构象,为新药结构优化提供了丰富的分子骨架选择。
咪唑并吡啶衍生物在药理学研究中展现出多样的生物活性,可作为抗癌、抗真菌、抗炎及镇痛类药物的重要先导结构。如有研究者合成了一系列四唑稠合咪唑并吡啶衍生物(12a–j),并系统评估其对三种人类癌细胞系(包括乳腺癌 MCF-7、MDA-MB-231 以及肺癌 A549)的抑制活性。结果表明,部分化合物的活性均显著优于阳性对照阿霉素,显示出良好的进一步开发潜力[1]。
金属腐蚀是金属材料在环境中发生化学或电化学反应并逐渐劣化的过程,其本质是金属向热力学更稳定的化合态转变。在工业体系中,低碳钢、铜及其合金因其优良的力学性能与加工性能而被广泛使用,但在酸性介质中均具有较高的腐蚀敏感性。特别是在采用盐酸进行酸洗或除垢的过程中,金属表面易遭受严重腐蚀,从而导致设备寿命缩短及潜在安全隐患。
为减轻酸性环境中的腐蚀作用,添加缓蚀剂是最有效且经济的防护策略之一。研究表明,有机缓蚀剂因其高效、低毒、易分散以及成本适中等优势,在金属腐蚀防护领域得到广泛应用。这类缓蚀剂通常含有杂原子、极性基团、芳环或具有孤对电子与π电子的结构单元,可通过与金属表面发生吸附作用形成稳定的保护膜,从而有效抑制腐蚀反应。
文献显示,咪唑并吡啶类化合物具有优异的缓蚀性能,近年来逐渐成为酸性介质中金属腐蚀抑制剂研究的热点。Lamghafri 等人研究了一种新型咪唑并吡啶衍生物 — (Z)-N-(4-(二甲氨基)亚苄基)-7-甲基-2-苯基-1,5-二氢咪唑并[1,2-a]吡啶-3-胺,并在 1 M HCl 电解液中评估其对铜(Cu)和低碳钢(MS)的缓蚀效果。研究采用了恒电位极化(PDP)、电化学阻抗谱(EIS)等电化学方法分析其缓蚀行为,同时利用扫描电子显微镜(SEM)观察金属表面形貌,并结合密度泛函理论(DFT)与蒙特卡罗(MC)模拟探讨抑制剂的吸附机制。
PDP 分析结果显示,铜样品在相同条件下表现出更优的耐腐蚀性,同时该咪唑并吡啶衍生物主要通过抑制析氢反应(酸性体系中的主要阴极反应)实现缓蚀,而对金属阳极溶解影响较小。吸附参数计算表明,该化合物可通过形成稳定的化学吸附层与金属表面强结合。总体来看,该咪唑并吡啶衍生物是一种高效的低碳钢和铜缓蚀剂,其吸附与缓蚀机理研究为设计新型有机缓蚀剂提供了重要参考[2]。
咪唑并[1,2-a]吡啶类化合物是一类典型的含氮稠合芳香杂环,因其独特的电子结构、稳定的芳香骨架以及易于功能化的特性,在药物化学、材料化学及金属离子传感等领域受到广泛关注。其多样的结构可通过引入不同官能团调控理化性质,使其具备抗菌、抗病毒、抗癌等生物活性,并可作为比色和荧光探针用于识别多种金属离子。
特别是含硫或含氮/硫官能团的咪唑衍生物,在金属配位方面表现更强,因此能增强对过渡金属离子的选择性。研究表明,含 N 或 S 的衍生物还可能具有更优的抗菌活性和更好的 ADMET 性能。
基于这些特点,研究者成功合成并表征了咪唑并吡啶衍生物 TIPA。TIPA 含有 N/S 配位基团,对 Cu²⁺ 显示出高选择性和高灵敏度(检测限 44.7 nM),并可产生明显的比色响应(由无色变为黄色)。抗菌活性测试表明,TIPA 对金黄色葡萄球菌、粪肠球菌、铜绿假单胞菌、大肠杆菌及白色念珠菌均表现出抑制作用,最小抑菌浓度(MIC)为 32–64 mg/L,并产生清晰的抑菌圈。同时,TIPA 在高浓度下仅显示轻度溶血作用(最大溶血率为 5.04%)。ADMET(吸收、分布、代谢、排泄及毒性)模拟以及与 PBP2a 的分子对接结果进一步支持其良好的药代动力学性质和显著的靶点结合能力[3]。
综上,TIPA 兼具抗菌活性与金属离子识别能力,是一种具有药理学和光学双重意义的多功能咪唑并吡啶衍生物。
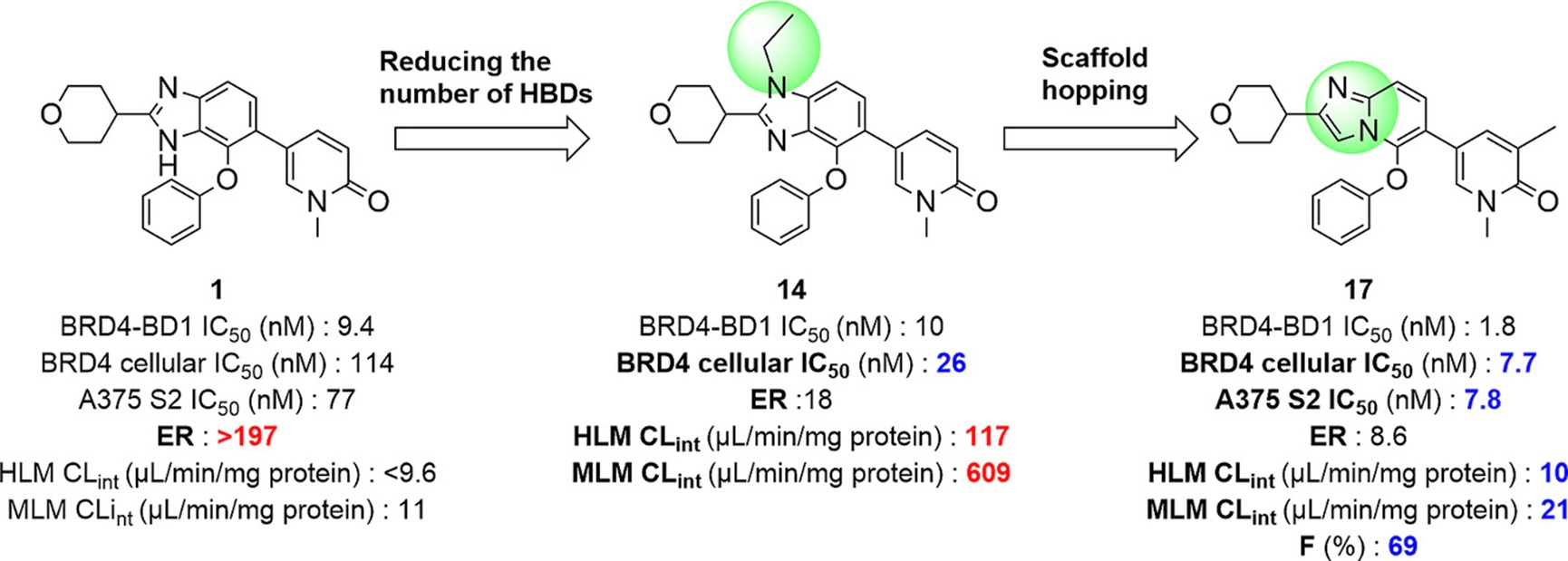
为提升 BRD4 抑制剂对黑色素瘤细胞的增殖抑制效果,研究者首先对某苯并咪唑衍生物 1 的构效关系(SAR)进行了系统研究,并希望筛选出在小鼠黑色素瘤异种移植模型中以较低剂量即可产生抗肿瘤作用的候选化合物。
研究团队设计了两项优化策略:增强 BRD4 抑制活性与提高细胞渗透性。通过对苯并咪唑核心进行 N-烷基化,减少氢键供体(HBD)数量,从而降低其被 P-gp 识别和外排的可能性,化合物的细胞增殖抑制活性得以提高。然而,此类化合物在代谢稳定性方面仍存在不足。
为克服这一缺陷,团队进一步采用骨架跃迁(scaffold hopping)策略,引入缺乏核心氢键供体的结构,最终获得了咪唑并吡啶衍生物 17。该化合物不仅表现出显著的抗黑色素瘤细胞增殖活性,还具有良好的口服药代动力学特性[4]。
c-Met 受体酪氨酸激酶在多条信号转导通路中发挥关键作用[1,2]。在正常生理状态下,其多效性受到严格调控。然而,大量研究表明,c-Met 在膀胱癌、乳腺癌、结直肠癌、胃癌和肺癌等多种肿瘤中存在异常激活[3–7],且其过表达或扩增通常与不良临床预后相关[8]。因此,c-Met 激酶已被认为是癌症治疗的重要靶点。
研究者合成并评估了一系列咪唑并吡啶衍生物(7a–7j)对 c-Met 的抑制作用。结果显示,大多数化合物在酶水平和细胞水平均表现出良好的抑制活性。其中,化合物 7g 的表现尤为突出,其对 c-Met 的 IC₅₀ 分别为 53.4 nM(酶水平)和 253 nM(细胞水平)。分子对接结果表明,7g 可能作为潜在的 c-Met 激酶先导化合物,值得进一步研究[5]。
此外,咪唑并吡啶衍生物在乳腺癌、胰腺癌及前列腺癌中同样表现出显著活性。在针对去势抵抗性前列腺癌(CR PCa)的研究中,研究者构建了一系列新型咪唑并吡啶衍生物,并在多种细胞系(包括 AR 阳性与 AR 阴性 AI PCa 细胞)中评估其作用。结果表明,该类化合物可抑制肿瘤细胞增殖,降低迁移能力并削弱体外致瘤性[6]。
综合已有研究,咪唑并吡啶类化合物在多个药理方向均展现出广泛活性,包括抑制多种靶向酶、抗病毒、抗细菌、抗微生物以及抗细胞增殖等。部分化合物已被用于开发治疗胃溃疡、糖尿病和精神疾病的药物,尤其在抗肿瘤研究中表现突出。因此,咪唑并吡啶是一类结构多样、应用广泛的重要含氮稠杂环化合物。
上海逐耀医药可提供多种含咪唑并 [1,2-a] 吡啶、咪唑并 [4,5-b] 吡啣、咪唑并 [4,5-c] 吡啶及咪唑并 [1,5-a] 吡啶骨架的化合物,供研究者进行新药研发。
[1] Vanam, Narendhar Reddy and Jaya Shree Anireddy. “Synthesis and Biological Evaluation of Tetrazole fused Imidazopyridine Derivatives as Anticancer Agents.” Chemical Data Collections (2023).
[2] Lamghafri, Selma et al. “Corrosion inhibition performance and adsorption properties of a novel imidazopyridine derivative for copper and mild steel in acidic medium.” Materials Today Communications (2025).
[3] Nandhagopal, Manivannan et al. “Anti-fungal effects of novel N-(tert-butyl)-2-(pyridin-2-yl)imidazo[1,2-a]pyridin-3-amine derivative and it’s in-vitro, in-silico, and mode of action against Candida spp.” Archives of Microbiology 206 (2024).
[4] Horai, Yuhei et al. “Discovering a potent and orally available imidazopyridine derivative as a BRD4 inhibitor: Enhancing antiproliferative activity against melanoma cells by mitigating P-gp substrate recognition.” Bioorganic & medicinal chemistry 129 (2025): 118337 .
[5] Yang, Yifei et al. “Discovery of imidazopyridine derivatives as novel c-Met kinase inhibitors: Synthesis, SAR study, and biological activity.” Bioorganic chemistry 70 (2017): 126-132 .
[6] Muniyan, Sakthivel et al. “Antiproliferative activity of novel imidazopyridine derivatives on castration-resistant human prostate cancer cells.” Cancer letters 353 1 (2014): 59-67 .
 沪ICP备2023026221号-1
沪公网安备 31011502400732号
沪ICP备2023026221号-1
沪公网安备 31011502400732号